このページの要点は以下のとおりです。
・話題の新薬エンハーツが鳴り物入りで承認された
・乳がんの第三次治療以降の選択肢としては高い有効性が期待されている
・特定された副作用の間質性肺疾患は日本人では特に気を付けて
・ILDはCOVID-19の症状と似ているので流行下では十分注意
今回は2020年5月20日に薬価収載の乳がん治療薬エンハーツ点滴静注用100mg(トラスツズマブ デルクステカン)について、審査報告書から紹介します。
ちなみにエンハーツは2020年9月には胃がんの適応が追加になっています。
【この記事を書いた人】

病院薬剤師です。DI関連の仕事で新薬の情報はちょこちょこ。
エンハーツはどんな薬?


いわゆるハーセプチン(トラスツズマブ)に抗悪性腫瘍薬デルクステカンを結合させた薬です。ADCは抗体薬物複合体のことです。
類似薬にカドサイラ(トラスツズマブ・エムタンシン)があります。
エンハーツは条件付き早期承認制度適用医薬品です。
承認条件として、現在実施中の第Ⅲ相試験の結果を早期に収集すること、となっています。
米国FDAでも、画期的治療薬(Breakthrough Therapy)指定やファストトラック指定(どちらも迅速審査、早期承認のための制度)を受けています。かなり期待されている薬のようですね。
エンハーツの有効性

国際共同第Ⅱ相試験(U201試験)の結果をもとに評価されています。
対象はカドサイラ治療歴のあるHER2陽性の手術不能又は再発乳癌患、主要評価項目はRECIST ver1.1 に基づく ICR判定による奏効率です。
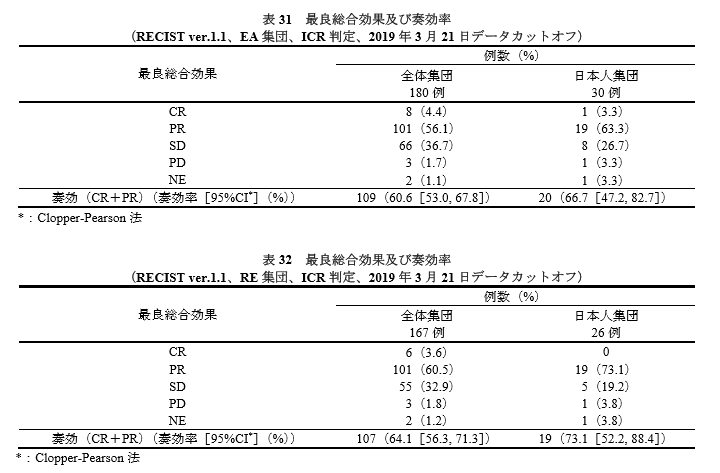
奏効率(CR+PR)は約6割と臨床的に意義のあるものであり、日本人患者においても同様の傾向があると記載されています。
第三次治療以降の治療であることを考えるとかなり高い奏効率と言って良さそうです。
また、パージェタ(ペルツズマブ)による治療歴や前治療歴にかかわらず、(カドサイラによる治療歴のある HER2 陽性の手術不能又は再発乳癌患者に対する)エンハーツの腫瘍縮小効果が認められた、と記載されています。
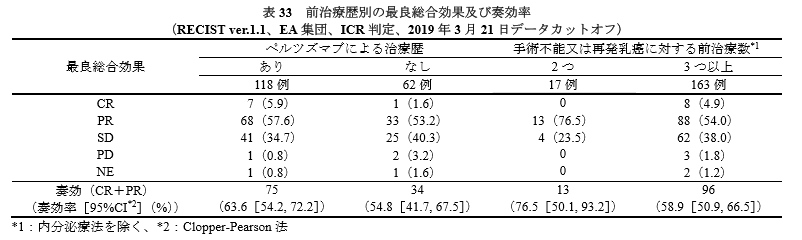
これらの結果を受けて、機構は以下のように判断しています。

エンハーツは、手術不能または再発乳がん患者に対する奏効率が、既存の薬剤よりも明らかに高いこと、カドサイラとは異なる機序の薬物が使用されている、という点で評価されています。
ちなみにWaterfall plotはこちら。

ほとんどの患者で縮小効果が見られているということを示しています。
エンハーツの相互作用
CYP3A代謝がメインと書かれており、イトラコナゾールやリトナビルとの併用時の血中濃度の変化が検討されていますが、CYP3A4阻害薬の影響はさほど受けないようです。
エンハーツの肝機能障害患者への影響

軽度・中等度の肝機能障害のある患者に対する投与量の調節は必要ないとのことですが、重度の肝機能障害がある場合は注意喚起をする旨が記載されています。Child-Pugh分類がAまたはBまでは使用可能と考えて良さそうです。
エンハーツの腎機能患者への影響

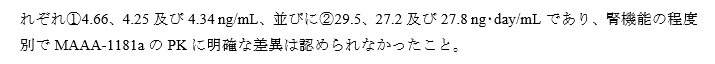
腎機能障害のある患者に対する臨床試験は行われていないとのことですが、この結果からは腎機能の低下を懸念する必要はあまりなさそうです。
エンハーツの安全性

RMP(医薬品リスクマネジメント計画)は以下のように設定されています。
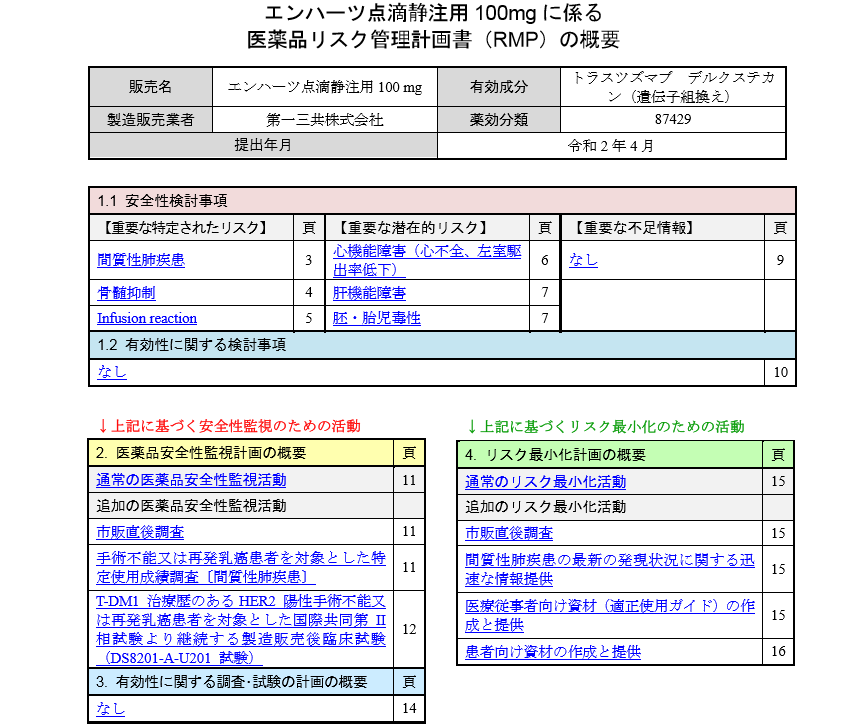
本薬投与時に特に注意を要する有害事象は、ILD、骨髄抑制、IRR、肝機能障害及び心臓障害である(p44)と記載されています。特に重要な副作用は間質性肺疾患(ILD)です。少し詳しく見ていきます。
間質性肺疾患(ILD)
ILD発現状況の国内外差
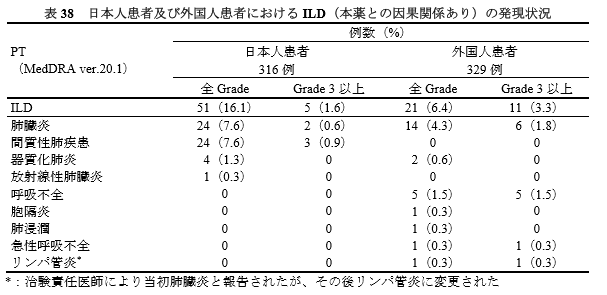
「本薬投与によるILD は外国人患者と比較して日本人患者において発現率が高かったこと(7.R.3.2 参照)等を考慮すると、日本人患者に本薬を投与する際にはILD の発現に特に注意が必要である。」(p52)と記載があります。
また次の表では、全Gradeでは16.1% vs 6.4%と日本人患者のほうが発現率が高いように見えますが、Grade3以上では1.6% vs 3.3%と逆の結果になっています。
日本人ではILD疾患のほとんどが肺臓炎、間質性肺疾患に偏っているように見えなくもないです。
ILDの画像上の特徴
P50 に以下のような記載があります。
Grade3未満のILD56例のうち48例は器質化肺炎類似型 (→未回復の症例が多い)
Grade3以上のILD16例のうち14例はびまん性肺胞障害型
ILDの画像パターンと重症度の間に一定の関連はありそうだが、転帰との関連性までは結論づけることはできない
Gradeが低くても未回復の症例が多いというのは気になりますね。
ILDのリスク因子
リスク因子については、メーカー側は以下のように説明しています。

これらの点から、ILDへの対応として以下のことが求められています。
・本薬の投与開始前には、ILD の合併及び既往歴の有無等を確認し、適応患者の選択を慎重に行うこ と。
・本薬の投与中は、臨床症状や SpO2、CT を含む画像検査等のモニタリングを継続的に行い、CT 画像 については専門医による診断を行うこと。
・ ILD が疑われる臨床症状等が発現した場合には、呼吸器専門医と連携し、本薬の投与中止、ステロ イド投与等の適切な対応を行うこと。
ILDに関しては、2019年5月に乳がん治療薬ベージニオ(アベマシクリブ)でブルーレターが発出されています。
販売後半年間で14例/2000例に重篤なILDが報告されていますので、エンハーツで同じ状況にならないように、資材を用いた十分な患者説明と投与後の副作用モニタリング等が重要と思います。
その他の副作用
その他、骨髄抑制、IRR、肝機能障害、心臓障害、消化管障害、QT延長、腫瘍崩壊症候群について確認しましたが、特別既知のリスクを大きく超えるものはなさそうな印象です。
エンハーツの臨床的位置づけ
一次治療における標準的な治療であるハーセプチン及びタキサン系抗悪性腫瘍剤を含む化学療法、二次治療における標準的な治療であるカドサイラより優先して本薬を使用することはできません。
また、現時点でタイケルブ/ゼローダ、ハーセプチン/セローダ療法等との使い分けについては不明です。

COVID-19流行下におけるエンハーツによる治療の留意点について
執筆時点(2020年5月19日)におけるトピックスです。

エンハーツによるILDとCOVID-19の胸部画像所見及び症状類似点がみられるため、鑑別のための検査(SARS-CoV-2のPCR検査等)が重要と記載されています。
また、ステロイドによる治療はCOVID-19に効果があるかどうかについて一定の見解は得られていないため注意が必要です。
また、個人的に気になったのは、

クロロキン/ヒドロキシクロロキンとエンハーツの作用が拮抗する可能性があることについては全く知りませんでした。
今後添付文書の改訂があるかもしれませんね。
カドサイラでも同様なのか?というのは気になります。
まとめ
・話題の新薬エンハーツが鳴り物入りで承認された
・乳がんの第三次治療以降の選択肢としては高い有効性が期待されている
・特定された副作用の間質性肺疾患は日本人では特に気を付けて
・ILDはCOVID-19の症状と似ているので流行下では十分注意

エンハーツは乳がん以外にも非小細胞肺がん、胃がんでも適応拡大していく方針のようです。
期待されている新薬だけに、販売後のILD含む副作用の発現状況は注視していきたいですね。
【関連記事】【胃がん適応も追加に】エンハーツの気になる副作用は?
審査報告書・RMPを利用した新薬の情報収集についてはこちらの記事もどうぞ




コメント